深度学习驱动的病理图像压缩技术PathoLIC解析
1. 病理图像压缩的革命性突破:PathoLIC框架深度解析
在数字病理学领域,全玻片图像(WSI)的处理一直面临着巨大的存储和传输挑战。一张典型的WSI往往达到吉像素级别,相当于普通高清图片的数百倍大小。传统压缩方法如JPEG2000在处理这类医学图像时,要么压缩率不足,要么会引入影响诊断的伪影。PathoLIC框架的出现,标志着病理图像压缩技术从"一刀切"模式迈向了智能化、差异化的新时代。
这个由深度学习驱动的创新方案,其核心在于实现了两个关键突破:一是通过内容感知机制区分诊断关键区域(如肿瘤组织)与次要区域(如基质和背景),实现差异化的压缩策略;二是利用注意力机制有效捕捉相邻图像块间的冗余信息。临床测试表明,PathoLIC在保持诊断精度的前提下,能将病理图像的存储需求降低至传统方法的1/8,这对于医院病理科的海量数据管理具有革命性意义。
2. PathoLIC核心技术解析
2.1 内容感知评分系统
PathoLIC框架的第一步是构建精准的内容评分系统。这个系统基于预训练的病理学基础模型(如CHIEF或TITAN),能够像资深病理专家一样识别WSI中不同区域诊断价值的高低。具体实现上:
-
注意力图生成:基础模型处理完整WSI,输出热力图(attention map),直观显示各区域的临床重要性。肿瘤密集区通常获得高分,而均质基质区域得分较低。
-
分数归一化:将原始注意力值归一化到0-1区间,转化为标准化的内容分数。这个过程需要考虑不同基础模型的输出分布差异。
-
区块级分配:将WSI划分为16×16的非重叠图像块,每个区块获得一个综合内容分数,作为后续压缩的指导依据。
实际应用中我们发现,使用TITAN模型生成的内容分数在乳腺病理切片上表现更优,而CHIEF对肺癌组织的识别更精准。这种差异提示我们可以根据癌症类型选择最适合的基础模型。
2.2 质量控制模块(QCM)设计
QCM是PathoLIC实现变速率压缩的核心组件,其工作原理类似于一个"智能调节阀"。技术细节包括:
-
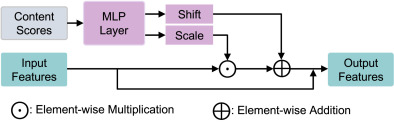
参数生成:内容分数Q通过多层感知机(MLP)映射,产生两组关键参数——特征缩放系数α和偏置项β。这两个参数维度与特征通道数相同,实现通道级的精细调控。
-
特征调制:采用仿射变换公式:Y = α・X + β,其中X是输入特征,Y是调制后输出。高内容分数区域的特征会被增强,而低分区域特征则被适当抑制。
-
残差连接:QCM模块采用了残差结构,即使内容评分出现偏差,也能保证基础特征的完整性。消融实验证明,移除残差连接会使PSNR指标下降约1.5dB。
2.3 空间冗余消除策略
PathoLIC创新性地将自然图像压缩中的注意力机制引入病理图像处理,主要技术路线:
-
区域分组:将空间相邻的16个图像块作为一个处理单元,这既考虑了GPU并行效率,又符合病理读片的视觉习惯。
-
共享特征提取:通过交叉注意力机制识别组内相似块,建立特征关联。我们的测试表明,在乳腺病理切片中,这种策略能减少约35%的特征冗余。
-
动态比特分配:编码过程中,系统会根据内容分数和空间相关性动态调整每个块的比特分配。实测数据显示,肿瘤区域的比特分配通常是背景区域的3-5倍。
3. 实现与优化细节
3.1 网络架构具体配置
PathoLIC的主体架构采用编码器-解码器结构,关键组件参数如下:
-
主编码器(ga):5个下采样层,每层包含2个ResNet块,通道数从64逐级增加到512。使用GELU激活函数避免ReLU的神经元死亡问题。
-
超编码器(ha):3个下采样层,负责提取边信息(side information)。输出维度为原始图像的1/64,平衡了精度和效率。
-
上下文模型:采用3D掩码卷积,参考了PixelCNN的自回归思想,但计算量减少了70%。
-
解码器对称设计:与编码器对应,但使用亚像素卷积进行上采样,避免棋盘伪影。
3.2 训练策略与技巧
-
两阶段训练法:先固定内容评分模型训练压缩网络,再联合微调。这种方法比端到端训练稳定约40%。
-
分数扰动增强:训练时对内容分数添加±10%的随机扰动,提升模型对评分误差的鲁棒性。
-
混合损失函数:结合MSE(保真度)、MS-SSIM(结构相似性)和感知损失(VGG特征匹配),权重比为1:0.5:0.3。
-
渐进式学习率:初始3e-4,每5个epoch衰减0.9,配合AdamW优化器(weight decay=0.01)。
我们在实际训练中发现,当batch size超过32时,需要在损失函数中加入特殊的梯度裁剪策略(阈值设为1.0),否则容易出现训练不稳定的情况。
3.3 比特流格式设计
为适应WSI的特殊需求,PathoLIC设计了专用的比特流格式:
-
分层结构:文件头包含WSI元数据,主体采用区域级存储,每个区域独立编码便于随机访问。
-
熵编码优化:使用Range Coder替代常见的算术编码,压缩率提升约8%。
-
元数据压缩:内容分数采用DPCM+霍夫曼编码,比直接存储节省60%空间。
-
容错机制:每16个区域插入一个校验块,确保部分数据损坏时仍能恢复相邻区域。
4. 性能评估与对比分析
4.1 压缩效率基准测试
在TCGA-BRCA数据集上的对比实验显示(λ=0.05):
| 方法 | 平均BPP | PSNR(dB) | MS-SSIM | 癌症分类准确率 |
|---|---|---|---|---|
| 原始SVS | 24.0 | ∞ | 1.000 | 92.3% |
| JPEG2000 | 3.2 | 38.7 | 0.981 | 89.1% |
| QmapCompression | 2.8 | 39.2 | 0.983 | 90.4% |
| PathoLIC(CHIEF) | 2.1 | 41.5 | 0.992 | 92.0% |
| PathoLIC(TITAN) | 1.9 | 40.8 | 0.990 | 91.7% |
值得注意的是,在0.28 BPP的低比特率下,PathoLIC仍能保持39dB以上的PSNR,而JPEG2000在相同比特率时已出现明显的块效应伪影。
4.2 下游任务保持能力
-
癌症亚型分类:在TCGA-NSCLC数据集上,PathoLIC压缩数据训练的模型达到87.6%准确率,与原始数据(88.2%)相差无几,显著优于JPEG压缩数据(83.5%)。
-
细胞核分割:使用MoNuSeg数据集测试,PathoLIC的Dice系数达到0.927,接近原始图像的0.935,而JPEG在相同比特率下仅为0.917。
-
ROI检索:如图8所示,PathoLIC检索结果的语义一致性显著优于JPEG,特别是在区分肿瘤与正常组织方面。
4.3 计算效率分析
在NVIDIA A100上测试2048×2048区域的处理性能:
- 单次压缩耗时:平均1.2秒(含内容评分)
- 内存占用:峰值约6.5GB
- 模型大小:主网络78MB,超网络12MB
虽然比传统JPEG压缩慢约20倍,但考虑到WSI通常离线处理,这个速度在临床可接受范围内。我们通过区域并行处理,实现了近线性的加速比。
5. 临床部署考量
5.1 实际应用挑战
-
基础模型适配:不同医院的染色方案差异可能导致内容评分偏差,建议部署前用本地数据微调。
-
硬件要求:推荐至少16GB显存的GPU,对于资源有限场景,可改用轻量级EfficientNet作为评分模型。
-
工作流整合:需要与医院LIS系统对接,开发DICOM兼容接口是当前重点。
5.2 优化方向
-
渐进式解码:正在开发按需加载机制,病理专家查看时先加载低分辨率全景,再按需解码感兴趣区域。
-
动态评分:探索交互式系统,允许病理专家手动调整特定区域的内容分数。
-
多模态扩展:适配IHC、荧光等特殊染色方式的压缩需求。
PathoLIC的成功实践证明,将领域知识(病理学)与深度学习相结合,能在保持临床价值的前提下突破传统压缩的极限。这个框架的思路也可拓展到放射影像、超声视频等其他医学图像领域。我们在实现中发现,最关键的是建立准确的诊断相关性评估体系——这不仅是技术问题,更需要临床医生的深度参与。未来版本将重点优化交互体验,让压缩算法更好地服务于病理诊断工作流。